| がん疾患名 | 肺がん | |
|---|---|---|
| 主診療科 | 呼吸器内科、呼吸器外科、腫瘍内科 | |
| 診療科 | 連携内容 | 目的 |
|---|---|---|
| 放射線科 | 診断・治療 | 併用によるがん治療 |
| 臨床病理科 | 病理診断 | 病理診断 |
| 緩和ケア科 | 緩和サポート | 身体的苦痛・精神的苦痛等の緩和 |
| 在宅医療部 | 在宅医療対応 | 在宅医療・在宅看護の実施 |
| 麻酔科 | 麻酔 | 手術時麻酔 |
| サポート | 連携内容 | 目的 |
|---|---|---|
| リハビリ | リハビリ | 身体機能の回復に向けたリハビリテーション |
| 臨床心理士 | 診療サポート | カウンセリングの実施 |
| 栄養士 | 栄養指導 | 栄養管理指導 |
| 薬剤師 | 医薬品の供給・情報提供 | 医薬品の調剤及び指導・相談など |
| NST | 栄養摂取 | 栄養摂取サポート |
| 禁煙外来 | 禁煙サポート | 禁煙に向けた薬物療法およびカウンセリング |
呼吸器内科の診療で最も大きな比重を占めるのが、肺がんの診断及び薬物治療(殺細胞性薬や分子標的薬、免疫チェックポイント阻害薬)です。診断には気管支鏡下生検とCTガイド下生検の二つがあり、最も合併症の少ない気管支鏡下生検は全て呼吸器内科が行っており、約530件(2018年度)と国内トップクラスに位置します。2011年より超音波気管支鏡(EBUS; Endobronchial Ultrasound)をほぼ全例に用いて生検を行うことで、高い組織診断率と正確な病理学的な病期分類が得られています。CTガイド下生検は気管支鏡下生検が困難な症例のみを放射線科医が行っています。これらより得られた生検材料より正確な組織診断・遺伝子学的診断(EGFR遺伝子変異、ALK、ROS1融合遺伝子異常、BRAF遺伝子変異)を行い、個別化医療(テーラーメイド医療)の実践に繋げています。また同時に腫瘍免疫療法(nivolumab、pembolizumab、atezolizumab、durvalumab)にも繋げられるようにPD-L1(Programed Death Ligand-1)検査を院内でほぼ全例に行っています。また週1回の頻度で肺がんカンファレンス(Lung Cancer Tumor Board)を呼吸器内科・呼吸器外科・放射線治療・腫瘍内科・がん化学療法認定看護師と合同で行い、連携を密にして集学的がん診療を目指しています。患者さまによっては、次世代シーケンシング(NGS; Next Generation Sequencing)を用いた網羅的遺伝子解析とエキスパートパネルを実施し、標準的治療以外に他の治療選択肢がないか、検索します。
各診療科と既に構築された連携をさらに強化し、連携チームによる集学的がん診療を今後も継続的に推し進めます。
肺がんは元より、非腫瘍性疾患にも積極的に取り組んでいます。
早期の肺がんに対しては縮小手術や胸腔鏡手術を行い、肺機能を温存し術後の痛みを軽減します
進行している肺がんでも、他の臓器に転移が無ければ放射線や化学療法を組み合わせて可能な限り切除します。
入院の待機期間は2週間から4週間ほどで、迅速な入院治療が可能です。
肺がん患者においては手術以外にも放射線・化学療法も専門医が治療します。
私どもの得意とする疾患に対する具体的な診断、治療方法を疾患ごとに述べます。 詳しくは、治療をご覧下さい。
患者さまの状態に即した手術を行うのはもちろんのこと、術後の生活に配慮した根治性の高い治療を提供していきたいと考えています。
肺がん以外にも様々な肺の病気を見つけるための基本検査です。肺がんについてはがんの大きさや拡がりなどを大まかに予測することができます。
喀出された痰のサンプルを顕微鏡で観察し、がん細胞の有無を調べる検査です。肺扁平上皮がんなどの中枢型肺がんや腺がんの特殊型である浸潤性粘液産生腺がんなどの発見には有効な場合があります。
胸部の体内領域を様々な角度から撮影して、精細な連続画像を作成して異常がないかを調べる検査です。画像はX線装置に接続されたコンピュータによって作成されます。病変の性状や形状の詳細な観察、縦隔・肺門リンパ節転移の有無、周辺臓器への浸潤の有無を確認するため、可能な限り造影剤の静脈内注射をして行います。
当院は日本呼吸器内視鏡学会認定施設であり、指導医・専門医が複数名在籍しています。2010年11月より仮想気管支ナビゲーション(VBN; Virtual Bronchoscopic Navigation)と超音波気管支鏡(EBUS; Endobronchial Ultrasound)を導入しました。ガイドシース併用気管支腔内超音波断層法(EBUS-GS)や超音波気管支鏡ガイド下針生検(EBUS-TBNA)が気管支鏡下生検のほとんどを占めています。2014年1月には検査数の右肩上がりの増加に対応するべく、また侵襲度の高い内視鏡治療が行えることをコンセプトにInterventional Pulmonology Suiteを内視鏡・診断治療センターの中に新設しました。最新Cアーム型X線透視装置を中央に配置し、術者右サイド6画面、左サイドに1画面、計7画面のディスプレイを配置し、特に6画面ディスプレイは天井吊り可動式にしました。これら検査室内の環境整備により内視鏡診断・治療が格段に行いやすくなりました。
以前はがんの縦隔リンパ節転移の有無を調べるのに縦隔鏡検査が行われましたが、現在は代わりに超音波気管支鏡ガイド下針生検(EBUS-TBNA)が普及しています。当院は現在約100件/年実施しています。縦隔鏡に比べて低侵襲であり、複数回の施行が可能であることは長所であり、また診断能においても遜色なく優れています。
この方法に仮想気管支ナビゲーション(VBN; Virtual Bronchoscopic Navigation)をほとんどのケースに併用することで、肺野末梢小型肺がんに対しては約80%以上と極めて高い診断率が得られています。
胸郭内病変(胸膜や肺内の結節)に対しCTをガイドに用いた経胸壁針生検です。特に小型肺がんの場合には気管支鏡下生検よりも診断率は勝りますが、合併症率は高くなります。
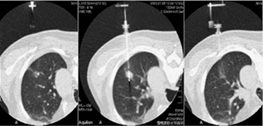
がんが疑われる体表面にあるしこり(結節・腫瘤)や腫れたリンパ節などに針を穿刺し、内部の組織や細胞を吸引採取する方法です。採取されたサンプルでがん細胞の有無を確かめます。
可能な限り、頭部造影MRIを行いますが、医学的な事情により行えない方には代わりに頭部造影CT検査を行います。脳を含めた頭部への転移の有無を調べるのが目的です。
腹部臓器への転移の有無を調べますが、消化管内病変を調べるのに胃・大腸カメラなどが必要になります。
肺がんの転移(縦隔・肺門リンパ節転移や全身臓器へのがんの拡がり)の有無を調べることができます。ただし、微小な脳転移などは頭部造影MRI検査でしか見つけることができず、また消化管内への転移検索には胃・大腸カメラなどが必要になります。
現在ほとんどの場合にはPET-CTで骨転移の有無を調べられますが、MRI検査や骨シンチグラフィー検査を追加で行うこともあります。
肺がんは、がん細胞の増殖や転移の性質と治療に対する反応性により、小細胞肺がんと非小細胞肺がんの二つに大別されます。さらに非小細胞肺がんは、扁平上皮がん、腺がん、大細胞がんの三つに別けられます。
詳細は治療のページをご参照ください。重喫煙者に多い肺がんであり、増殖スピードが早く転移を来たしやすい性質の肺がんであるため、手術適応になる患者さまは稀です。ですが、非常に抗がん薬(殺細胞性薬)や放射線治療に対する感受性の高い肺がんでもあります。大きく限局型と進展型に分けられ、初期治療として限局型にはプラチナ製剤併用抗がん薬と胸部放射線治療が同時に行われます。進展型にはプラチナ製剤併用抗がん薬と免疫チェックポイント阻害薬での治療が行われます。臨床病期I期の限局型である場合には、外科切除後にプラチナ併用抗がん薬を投与します。
病期分類(TNM分類)に準拠して治療方針を決定します。外科手術(+/- 術後抗がん薬)、術前抗がん薬→外科手術、術前抗がん薬 + 放射線治療→外科的切除、定位放射線治療、凍結治療、全身薬物治療(抗がん薬、分子標的治療、免疫チェックポイント阻害薬、またはこれら複数併用など)など非常に多岐に渡ります。非小細胞肺がん、とりわけ肺腺がんの全身薬物治療は病理組織型・免疫組織化学染色パターン・ドライバー遺伝子変異の有無(強力にがん化に関わる遺伝子変異)により治療体系が別れ非常に複雑化してきています。詳細は治療のページをご参照ください。
肺がんのステージ分類は胸部造影CT、FDG-PET、頭部造影MRI等の画像検査からTNM (Tumor-Node-Metastasis) 分類第8版を使用して臨床病期を決めていますが、Nステージに関しては超音波気管支鏡ガイド下針生検(Endobronchial Ultrasound guided Transbronchial Needle Aspiration; EBUS-TBNA)を積極的に行い正確な臨床病期を決定した上で方針決定に役立てています。
| Tis | 上皮内がん |
|---|---|
| T1mi | 微小浸潤性腺がん |
| T1a | 腫瘍の最大径≦1㎝ がん浸潤が葉気管支より中枢に及ばない |
| T1b | 1cm<腫瘍の最大径≦2㎝ がん浸潤が葉気管支より中枢に及ばない |
| T1c | 2cm<腫瘍の最大径≦3㎝ がん浸潤が葉気管支より中枢に及ばない |
| T2a | 3cm<腫瘍の最大径≦4cm もしくは下記のいずれかを伴う ①主気管支に浸潤が及ぶが、腫瘍の中枢側が気管分岐部には及ばない ②臓側胸膜に浸潤する腫瘍 ③肺門まで連続する部分的または一側全体の無気肺か閉塞性肺炎がある |
| T2b | 4cm<腫瘍の最大径≦5cm もしくはT2aの①-③を伴う |
| T3 | 5cm<腫瘍の最大径≦7cm または充実成分径≦5cmでも次のいずれかに直接浸潤する腫瘍;胸壁、壁側胸膜、横隔神経、縦隔胸膜、心膜;または原発巣と同一肺葉内に不連続な副腫瘍結節 |
| T4 | 充実成分径が7cm超 または大きさを問わず次のいずれかに浸潤する腫瘍;横隔膜、縦隔、心臓、大血管、気管、反回神経、食道、椎体、気管分岐部;または原発巣と同側の異なる肺葉内の副腫瘍結節 |
| N0 | 所属リンパ節転移なし |
|---|---|
| N1 | 同側の気管支周囲、同側の肺門・肺内リンパ節への転移 |
| N2 | 同側縦隔リンパ節、気管支分岐下リンパ節への転移 |
| N3 | 対側縦隔、対側肺門、同側あるいは対側の前斜角筋、鎖骨上窩リンパ節への転移 |
| M0 | 遠隔転移なし |
|---|---|
| M1a | 対側肺内の副腫瘍結節;胸膜または心膜の結節、悪性胸水、悪性心嚢水がある |
| M1b | 肺以外の一臓器への単発遠隔転移がある |
| M1c | 肺以外の一臓器または多臓器への多発遠隔転移あり |
| 限局期 | 腫瘍が同一胸郭内に存在し、同側肺門リンパ節、両側縦隔リンパ節、両側鎖骨上窩リンパ節に限局している場合、悪性胸水、心嚢水を認めない場合 |
|---|---|
| 進展期 | 限局型を超えて腫瘍が存在する場合 |
気管支鏡下あるいはCTガイド下生検により肺がんの組織型診断を行います。また病期分類に関しては、頸部から骨盤までの造影CT、脳の造影MRI、FDG-PET等により決定し、これら組織型と病期分類を基に治療方針を決定します。以下に示すのは代表的な治療方法であり、患者さまの背景や全身状態、併存疾患などにより異なることもありますので、詳細は各担当医にご相談ください。
IA-B期→基本的には外科的切除を行います。併存疾患や低肺機能などの理由で外科的切除が困難な場合には定位放射線照射(Stereotactic Radiation Therapy; SRT)や凍結治療などを行うこともあります。外科的切除後のIB期には術後補助化学療法(UFT内服)を行います。
IIA-B期→基本的に外科的切除を行い、術後補助化学療法(プラチナ併用化学療法)を行います。場合によっては術前化学療法(プラチナ併用化学療法)後に外科的切除を行う場合もあります。IIB期のうち胸壁浸潤がん(T3)に関しては術前化学放射線併用療法(胸部放射線照射量;40-46Gy/20-23回)後に外科的切除を行います。
完全切除可能なIIIA(N2)期、胸壁浸潤がんを含む隣接臓器浸潤がん(T3-T4)→術前化学放射線併用療法(胸部放射線照射量;40-46Gy/20-23回)後に外科的切除を行います。また完全切除不能なIIIB、IIIC(N3)期には基本的に根治的化学放射線併用療法(胸部放射線照射量;60Gy/30回)を行いPD-L1阻害薬のデュルバルマブを投与します。完全切除が可能と判断されるIIIB、IIIC(N3)期には術前化学放射線併用療法後に外科的切除を行う場合があります。
ⅣA-B期→全身化学療法を行います。正確な組織型診断及び得られた遺伝子学的情報をもとに最適な個別化治療を行います(以下の「各治療の説明B 化学療法」をご参照ください)。
肺は右肺が上葉、中葉、下葉に、左肺は上葉、下葉の5つの房状(肺葉)に分かれており、病巣のある肺葉を切除する方法です。
当院では患者さまへの体の負担が軽減できるよう、小さな切開で開胸手術を行うことができる胸腔鏡を利用した胸腔鏡補助下手術(VATS:Video Assisted Thoracoscopic Surgery)を導入しております。
[肺葉切除術]
5cm以下の肺癌でリンパ節転移がない場合には標準手術として胸腔鏡下で肺葉切除を行っています。完全胸腔鏡下に行う肺癌手術は小さな創で行う事ができ痛みが少なく、手術からの早期回復が期待されます。
肺癌に対しては通常、肺葉切除という手術が行われますが、早期・小型肺癌に対して当科では肺を小さく切除する区域切除に積極的に取り組んでいます。全スタッフが最近4年間に経験した区域切除は300例を越えています。
肺葉切除が術後肺機能を約85%に低下させるのに比べて、区域切除は90〜95%ほどにしか低下しません。そのため区域切除の術後は肺葉切除に比べて体力の低下が少なくなります。術後生存率は、選択された症例において、区域切除は肺葉切除と同等の治療成績であることが発表されています。肺癌の性質やあなたの体力により肺葉切除がいいか区域切除がいいか判断されます。主治医とよく相談の上、決定します。
肺の周囲に浸潤している肺癌やリンパ節転移のある肺癌に対しては手術前に放射線療法と抗がん剤治療を行って、腫瘍を小さくして、腫瘍の勢いを弱めてから手術をした方が、術後の再発が少ないことが報告されています。放射線化学療法で腫瘍や転移が縮小した症例においては、約40%近い患者さんが長期生存されています。
小さな肺腫瘍は手術中に目で見ても触っても判らないことが多くあります。それに対して術前に色素と造影剤によるマークを行うことにより確実な切除を心がけています。
図は微小肺癌ですが、それに対して造影剤をCT室で病変に注入し、それをマークに切除した症例です。
気管や太い気管支に浸潤している癌は通常ですと手術不能、あるいは片肺全摘を必要とすることがありますが、私どもは気管・気管支の癌の浸潤部位のみを切除して肺を温存することを積極的に行っています。この手技は熟練を要しますが、私どもはその経験数が豊富です。
肺癌が隣の臓器に浸潤していても、切除可能であれば、拡大合併切除を積極的に行っています。心臓の一部、大動脈の一部さえも積極的に合併切除していておりますが、現在までに手術死亡はありません。
癌あるいは良性の瘢痕により気管あるいは気管支が狭窄をして息が辛くなる場合があります。それに対して私どもはステントの挿入やレーザー治療を多く手かげております。
昔に罹った膿胸(結核のことが多い)が何年も経過した後に再発した有瘻性(気管支と膿胸腔が交通すること)の場合には、内科治療ではまず治りません。当院では開窓術(胸壁を切除して、膿胸腔を開放すること)を行い、後に胸壁の筋肉、あるいはさらに皮膚をも用いて膿胸腔を充填することを行っています。特に筋弁もしくは筋皮弁を用いた膿胸根治法における当院の経験は豊富です。
多くの種類の癌が肺に転移をします。しかしある種の癌で、転移の個数が多くなく、原発巣が完全切除されている場合には、肺の転移巣を切除することにより治癒する、あるいは余命が延長することが知られています。
そのため「転移をしたからもうだめだ」とあきらめないで、肺転移巣が切除可能かどうか受診することが勧められます。
術後には望まない不都合な状況が発生することがあります。これを合併症といいます。特に高齢者、喫煙者、低肺機能症状を持つ患者さまは肺がんの術後合併症のリスクが高く、より一層の注意が必要とされています。
主な術後合併症として、胸に空気や水がたまりやすいことから、肺水腫、乳糜胸、膿胸、気管支瘻、肺炎などになるケースがあります。
また、これ以外にも、操作と直接関係なく発生する脳疾患や心疾患、麻酔薬や手術前後に投与された薬剤による肝機能障害などが起こることもあります。
これらの合併症については、発症を防げるようにスタッフ一同、術前および術後、細心の注意を払い診療及びケアに携わっておりますが、医療過誤や過失によるものではなく、一定の割合で発生してしまいます。心配な方は、担当の医師にお尋ねください。
当院では、手術(主に肺葉切除術)後も患者さまが日常生活において負担がかからないよう、呼吸器リハビリテーション担当の理学療法士による術前および術後の呼吸リハビリテーション(以下、リハビリ)を積極的に実施しております。
肺がんの手術(肺葉切除術)は手術1~3日前に入院していただくケースが一般的です。術前の1~3日間にリハビリの説明と術後のリハビリに向けた練習、現状の身体機能評価を行ないます。
そして、術後身体状況に問題がなければすぐに病室でリハビリを開始します。
ほとんどの患者さまが退院までに日常生活に支障がない程度の活動レベルに回復します。
入院から退院までの期間は約1~2週間程度です。
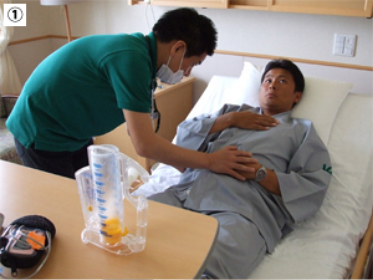
①横隔膜呼吸の練習
鼻から膨らませる様に空気を吸い、ゆっくり、深呼吸を行います。
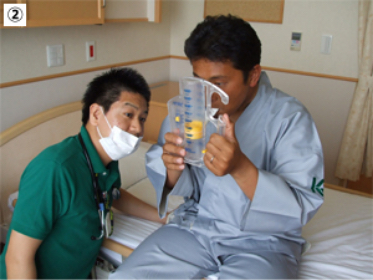
②練習器具
呼吸練習器具を用いて手術前より呼吸練習を行います。
手術後の肺合併症予防に有効です。

③術前より咳嗽方法を習得
術後、咳嗽力が低下し、自分で痰を出すことが困難になります。術前より咳嗽方法を習得することが大切です。
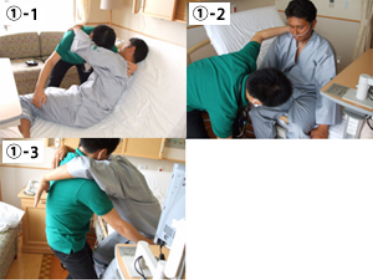
①歩行練習の開始
術後1~2日目より、理学療法士の指導・補助の下、歩行練習を始めます
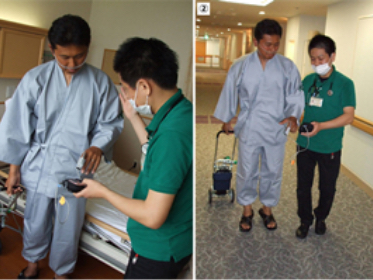
②歩行訓練
歩行訓練は病室、病棟廊下などを利用して血中酸素飽和度をチェックしながら行ないます。
また、痛みに関しては表面の傷の痛みはなくなっても肋間神経の痛みはしばらく残り、肩こりやしびれなども出現する場合がありますので、痛みを強く感じていらっしゃる患者さまへは鎮痛剤や安定剤の処方を行ないます。
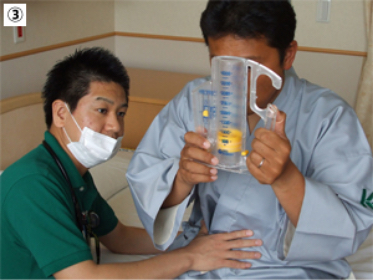
③肺の拡張を促す
術後早期から自分自身で練習を行い、肺の拡張を促します。
殺細胞性薬、分子標的薬、免疫チェックポイント阻害薬などがあります。非小細胞肺がんであれば、基本的に抗PD-L1抗体(22C3抗体)による免疫組織化学染色を行い腫瘍のPD-L1発現割合を調べた後に、免疫チェックポイント阻害剤(ニボルマブ・ペンブロリズマブ・アテゾリズマブ・デュルバルマブ)の投与を検討します。薬剤によってはPD-L1発現割合の計測は必須でありません。非扁平上皮・非小細胞肺がんであれば、ドライバーがん遺伝子(EGFR遺伝子変異、ALK・ROS1融合遺伝子異常、BRAF遺伝子変異)を可能な限り検索します。これらの情報によって個々の患者さまに個別化された適切な治療薬剤を提供します。遺伝子検査は有料で検査する内容により料金は異なってきます。詳細は各担当医にお尋ねください。
① 殺細胞性薬
一般的に抗がん剤と言われる薬剤です。注射薬と内服薬がありますが、多くは注射薬です。基本的に日常生活が自立し活動力のある方に適応となります。寝たきりの方など活動力が著しく低下している方に投与すると有害事象が強く出現し、逆に生命予後を短くしてしまう可能性が高くなるためお勧めしておりません。殺細胞性薬の有害事象としては血液毒性と非血液毒性に大別されます。血液毒性とは骨髄抑制による白血球、ヘモグロビン、血小板の減少です。悪化すると重篤な感染症、貧血や出血などを認めることがあります。他の特徴的な有害事象は欄に記載しましたが、その他にも様々な有害事象が発生する可能性があります。各薬剤により投与間隔や期間が異なるため詳細は各担当医にお尋ねください。
75歳未満
プラチナ製剤(主にシスプラチン) + 第3世代抗がん剤(±アバスチン)を併用投与します。投与方法は各殺細胞性薬により異なります。もちろん分子標的薬や免疫チェックポイント阻害薬に関しては適応があれば積極的な投与を行います。
75歳以上80歳未満
プラチナ製剤 + 第3世代抗がん剤を使用しますが、プラチナ製剤の場合にはカルボプラチンの使用が多くなります。患者さまの状態によっては第3世代抗がん剤のみを投与する場合もあります。その場合の有効性はプラチナ製剤併用時よりも劣ることになります。もちろん分子標的薬や免疫チェックポイント阻害薬に関しては適応があれば積極的に投与を行います。
80歳以上
殺細胞性薬に関しては、有効性・安全性を示す医学的根拠に乏しいため通常は行いませんが、高齢の方でも見た目年齢の若い方もいらっしゃるため、暦年齢のみで治療適応を決めるようなことはしていません。もちろん分子標的薬や免疫チェックポイント阻害薬に関しては適応があれば積極的な投与を考慮します。
| 商品名 | 一般名 | 特徴 | |
|---|---|---|---|
| 注射 | シスプラチン | シスプラチン | プラチナ製剤です。当院ではジェネリック医薬品を使用しています。 有害事象は腎毒性や嘔気、嘔吐等があります。腎毒性を予防するために3日間点滴をします。 |
| カルボプラチン | カルボプラチン | プラチナ製剤です。当院ではジェネリック医薬品を使用しています。有害事象は腎毒性や嘔気、嘔吐等があり、腎毒性はシスプラチンより少ないです。 | |
| アクプラ | ネダプラチン | プラチナ製剤です。 有害事象は腎毒性や嘔気、嘔吐等があります。ドセタキセルと併用し扁平上皮がんに使用します。 | |
| アリムタ | ペメトレキセド | 非扁平上皮・非小細胞肺がんに使用します。 有害事象はしびれや嘔気等があります。有害事象軽減のため葉酸とVB12の補充を行います。 | |
| ドセタキセル | ドセタキセル | 当院ではジェネリック医薬品を使用しています。有害事象としては骨髄抑制、消化器症状等があります。 | |
| パクリタキセル | パクリタキセル | 当院ではジェネリック医薬品を使用しています。有害事象としては投与時のアレルギー反応(発熱、呼吸困難、血圧低下)やしびれ等があります。 | |
| アブラキサン | Nab-パクリタキセル | パクリタキセルの製剤を加工し副作用を少なくした製剤です。 | |
| ゲムシタビン | ゲムシタビン | 当院ではジェネリック医薬品を使用しています。有害事象としては薬剤性肺障害や血小板低下等があります。 | |
| ビノレルビン | ビノレルビン | 当院ではジェネリック医薬品を使用しています。有害事象としては静脈炎等があります。 | |
| アバスチン | ベバシズマブ | 一般的には第3世代抗がん剤と併用して使用されます。有害事象としては高血圧、蛋白尿、出血等があります。 | |
| サイラムザ | ラムシルマブ | ドセタキセルと併用します。有害事象は蛋白尿、出血等があります。 | |
| 内服 | TS-1 | テガフール/ ギメラシル/ オテラシル |
内服薬です。有害事象は嘔気や下痢などの消化器症状です。 |
| UFT | テガフール・ウラシル | 内服薬です。術後に服用することが多いです。 |
② 分子標的薬
肺がんの発症に大きく関わる原因遺伝子にEGFR遺伝子変異、ALK、ROS-1融合遺伝子異常、BRAF遺伝子変異があります。これらがん化に強く関わる原因遺伝子を標的として治療する薬剤です。生検・手術で採取した組織検体、血液検体などを用いてこれらの原因遺伝子を調べます。結果が判明するのに約2-3週間程度かかります。治療薬は主に内服薬であり、また殺細胞性薬と比較し奏効ある確率は非常に高く、また概ね有害事象も少ないため通院治療が可能です。
| 商品名 | 一般名 | 特徴 | |
|---|---|---|---|
| 内服 | イレッサ | ゲフィチニブ | EGFR遺伝子変異陽性の方が対象です。有害事象は肝障害、皮疹、下痢、薬剤性肺障害等があります。 |
| タルセバ | エルロチニブ | EGFR遺伝子変異陽性の方が対象です。有害事象は肝障害、皮疹、下痢、薬剤性肺障害等があります。 | |
| ジオトリフ | アファチニブ | EGFR遺伝子変異陽性の方が対象です。有害事象はイレッサと類似していますが、下痢が他の薬剤よりも強く認められることがあります。 | |
| タグリッソ | オシメルチニブ | EGFR遺伝子変異陽性の方が対象で一番初めに使用する薬剤です。有害事象に皮疹、下痢、心電図異常があります。 | |
| アレセンサ | アレクチニブ | ALK融合遺伝子異常を有する方が対象です。 有害事象は味覚障害、発疹、便秘、消化管穿孔、薬剤性肺障害等があります。 | |
| ザーコリ | クリゾチニブ | ALKまたはROS-1融合遺伝子異常を有する方が対象です。 有害事象は視覚障害、下痢、浮腫、薬剤性肺障害等があります。 | |
| ジカディア | セリチニブ | ALK融合遺伝子異常を認め、クリゾチニブを内服し治療効果が認められなくなった方が対象です。 有害事象は悪心や嘔吐、下痢などの消化器症状や肝障害、薬剤性肺障害等があります。 | |
| タフィンラー/ メキニスト |
ダブラフェニブ/ トラメチニブ |
BRAF遺伝子異常を有する方が対象です。有害事象は発熱、消化器症状、皮疹、二次発癌、心障害等があります。 | |
| ロズリートレク | エヌトレクチニブ | NTRK融合遺伝子、ROS-1融合遺伝子異常を有する方が対象です。有害事象は味覚異常、めまい、末梢神経障害、下痢、認知障害、薬剤性肺障害等があります。 |
③ 免疫チェックポイント阻害薬
体の中にリンパ球という細胞が存在しますが、体内に異物が侵入した際にリンパ球が異物を認識し除去します。がん細胞は異物として認識されないよう工夫し体内で増殖します。再度、リンパ球にがん細胞を異物として認識させるようにする薬剤が免疫チェックポイント阻害薬です。使用に際しては採取されたがん組織検体にPD-L1発現の有無を確認します。PD-L1発現のない方は組織型によっては使用できない場合があります(詳細は各担当医にお尋ねください)。現在使用できる薬剤は全て注射剤であり、副作用の特徴は殺細胞性薬とは全く異なり、体の免疫機能を調整する薬剤であることから、様々な自己免疫に起因する有害事象が認められます。
| 商品名 | 一般名 | 特徴 | |
|---|---|---|---|
| 注射 | オプジーボ | ニボルマブ | 有害事象として糖尿病や重症筋無力症、甲状腺機能異常、薬剤性肺障害、薬剤性腸炎等があります。 |
| キイトルーダ | ペムブロリズマブ | 有害事象はニボルマブと同様です。 | |
| テセントリク | アテゾリズマブ | 有害事象はニボルマブと類似しています。また髄膜炎の有害事象があります。 | |
| イミフィンジ | デュルバルマブ | 非小細胞肺癌に対して根治的化学放射線療法を施行した方に投与します。詳しい適応は担当医にお尋ねください。 |
④ その他
| 商品名 | 一般名 | 特徴 | |
|---|---|---|---|
| 注射 | ポートラーザ | ネシツムマブ | 化学療法歴のない進行・再発扁平上皮肺癌に対して使用します。シスプラチン、ゲムシタビンと併用します。有害事象は皮膚障害、口内炎、血栓塞栓症などがあります。 |
肺がんにおいて放射線照射は有効な治療法で様々な使用法があり、目的に応じて根治的照射(完全治癒を目的)と緩和的照射(症状緩和を目的)があります。放射線は目的によって照射量が異なり、それによって照射日数も異なります。またがん周囲の臓器にも放射線がある程度照射されることにより障害が生じます。皮膚障害(皮膚が赤くなる)や食道炎(嚥下時に痛みを伴う)は照射中に認められます。また胸部照射中または照射6ヶ月後までに放射線性肺障害(発熱や咳、呼吸困難)が出現します。他にも心臓や脳にも障害が認められる時があります。
・定位放射線治療(Stereotactic Radiation Therapy; SRT); 数回に分割して照射を行う
・定位手術的照射(Stereotactic Radiosurgery; SRS); 1回で照射が完了する
早期の非小細胞肺がんに対し、何らかの医学的な理由で外科的切除が行えない場合の代替治療法として、呼吸同期体幹部SRTを行っています。また肺がんの脳転移に対して当院はSRTを行っていますが、γナイフ治療(コバルトから出るγ線を用いたもの)に代表されるSRSは当院で行えないため、千葉県循環器病センターや築地神経科クリニックのγナイフセンターに紹介させていただいています。
肺がんの脳転移に対しては可能な限りSRTやSRSを行いますが、転移の大きさや個数の多い場合には行えない場合があります。その際には脳全体に放射線照射を行う全脳照射(30Gy/10回)を行うことになります。急性期には嘔気や嘔吐、脱毛などの症状が認められ、照射後長期間経過した後の晩期毒性として物忘れなどの認知機能や下垂体機能の低下などが認められることもあります。
他にも、重粒子線治療(炭素線治療)や陽子線治療などもありますが、本邦では保険認可されておらず、当院では行っておりません。医学的適応があると判断した場合には実施可能な施設にご紹介させていただきます。
最近はCTにより超早期肺癌と言われる小さな肺癌や、他臓器の癌からの小さな肺転移が見つかるようになりました。その場合どの施設でも手術を優先されますが、亀田総合病院では凍結治療も行っています。同方法はCTを見ながら凍結針を腫瘍に刺して、針の温度をマイナス170度以下にして癌を死滅させる治療です。
亀田総合病院で行われる凍結治療は液体窒素を用いる方法です。従来の凍結治療はアルゴンガスを用いた方法です。一方、液体窒素を用いる凍結機器は近年開発されたものであり、アルゴンガスより強力な凍結能力を有し、2010年に米国のFDA(日本の厚生労働省に相当)で承認され、2011年より市場販売され始めました。当院では2013年11月から液体窒素を用いた凍結治療を原発性肺癌および転移性肺癌に対して行っており、2014年12月まで35人の患者さんに凍結治療を行ってきました。液体窒素を用いた凍結は凍結能力が高いので、通常は1本の凍結針で治療できます。
同治療は局所麻酔で約1時間かけて行う治療ですが、傷は針の孔だけなので術後の痛みはほとんど無く、通常治療後3-4日目には退院でき、退院後翌日からは通常の社会生活に復帰できます。そのため手術が困難であるといわれる高齢者あるいは体力に余裕のない患者さま、また手術を希望されない患者さまにはこの凍結治療を行っています。
凍結治療が適応となり得る腫瘍を以下に列挙します。
1. 腫瘍のサイズが原則として2cm以下の原発性肺癌あるいは転移性肺癌。
2. 病変の数が原則として1個あるいは2個。
3. 但し、病変が2個以上の多数の転移性肺癌でもその内の1-2個が大きく、大きな転移巣により余命が短くなる可能性がある場合には凍結治療の適応となり得ます。
4. 放射線治療後の肺病変の再発。
5. 呼吸機能の制限や癌の特性により手術療法が困難な場合。
*凍結治療は手術を行う事なく肺の悪性病巣を治療できる有用な方法です。手術ができない方やこれを回避したい方においては特にメリットの多い方法です。その反面、その効果・副作用に関するデータの蓄積が不十分です。それ故、保険適応ではなく自費診療となります。適応に関しては主治医と相談の上判断いたします。
現在まで治療した105人の患者さまの生存曲線を示しますが、現在まで90%以上の方が生存されています。
以下に局所制御率(*)を腫瘍のサイズ毎に紹介します。1cm以下では局所制御率は100%で再発はありません。1.1 - 2cmでは局所制御率は85%、2.1 - 3cmでは40%です。
*凍結治療を行った部位における再発の制御率
保険適用ではないので、自費診療となります。標準的な入院期間は7日間です。
費用は、入院治療費と入院された日数分室料が発生します。入院治療費には、入院治療費用+凍結針1本+食事療養費が含まれます。
・Kタワー入院の場合 入院治療費100万円+Kタワー室料(1日13,000円)+消費税
(Kタワーの場合、家族の方も泊まれます。)
・A棟入院の場合 入院治療費100万円+A棟室料(1日6,000円)+消費税
(例)6泊7日、Kタワー入院の場合
(1,000,000円+91,000円)x1.1 = 1,200,100円
入院治療費 室料 消費税
なお、腫瘍が大きい、あるいは腫瘍が2箇所ある場合には、凍結針2本します。その際には上記金額に15万円追加となります。
治療をご希望される方は、亀田総合病院(千葉県鴨川市)の水曜日午後、木曜日午前、第2・4土曜日午前の外来(医師、杉村裕志)あるいは亀田病院京橋クリニック(東京都中央区京橋)の土曜日(第1・3週目)午前の外来(医師、杉村裕志)を受診してください。
LD(限局型)
臨床病期I-ⅡAの方に手術適応があり、基本的に肺葉切除を行いますが、術後補助化学療法としてシスプラチン併用化学療法が必要になります。それ以上の病期のLDの方には根治的化学放射線併用療法を行います。しかし、これらの併用療法は有害事象が強く認められるため、患者さまの状態に応じて化学療法単独になる方もいます。根治的化学放射線併用療法により、寛解状態に入った方には予防的全脳照射を行います。
ED(進展型)
基本的に化学療法を行うことになりますが、状況によっては姑息的放射線照射を併用することもあります。
小細胞肺がんに使用する化学療法は殺細胞性薬のみです。基本的な副作用や薬剤投与該当患者は非小細胞肺がんに類似しています。
| 商品名 | 一般名 | 特徴 | |
|---|---|---|---|
| 注射 | シスプラチン | シスプラチン | プラチナ製剤です。当院ではジェネリック医薬品を使用しています。有害事象は腎毒性、嘔気や嘔吐等があります。腎毒性を予防するために3日間点滴をします。 |
| カルボプラチン | カルボプラチン | プラチナ製剤です。当院ではジェネリック医薬品を使用しています。有害事象は腎毒性、嘔気や嘔吐等があります。腎毒性はシスプラチンより少ないです。 | |
| エトポシド | エトポシド | 当院ではジェネリック医薬品を使用しています。有害事象として嘔気や嘔吐等があります。 | |
| カルセド | アムルビシン | 有害事象として嘔気や脱毛、不整脈等があります。 | |
| イリノテカン | CPT-11 | 有害事象として下痢などの消化器毒性や薬剤性肺障害があります。 | |
| テセントリク | アテゾリズマブ | ED型の小細胞肺癌の方でカルボプラチンとエトポシドと併用して使用します。免疫チェックポイント阻害薬です。 |
小細胞肺がんのLDには、プラチナ製剤(主にシスプラチン) + エトポシド併用化学療法と根治的な胸部放射線照射を同時に使用する根治的化学放射線併用療法を行います。腫瘍性の中枢気道狭窄や上大静脈症候群などによる呼吸困難及び骨転移による疼痛に対しては緩和的な放射線照射を行います。非小細胞肺がんのC 放射線治療もご参照ください。

医師 主任部長
中島 啓 (なかしま けい)
NAKASHIMA Kei
日本内科学会認定内科医・総合内科専門医、 日本呼吸器学会呼吸器専門医・指導医、 日本呼吸器内視鏡学会気管支鏡専門医・指導医、 日本感染症学会感染症専門医・指導医、 日本結核非結核性抗酸菌症学会結核・抗酸菌症認定医、 臨床研修指導医講習会修了、 緩和ケア研修会修了、 厚生労働省指定オンライン診療研修修了
医師の詳細はこちら
医師 部長
伊藤 博之 (いとう ひろゆき)
ITO Hiroyuki
日本内科学会認定内科医、 日本内科学会総合内科専門医、 日本呼吸器内視鏡学会気管支鏡専門医・指導医、 日本呼吸器学会呼吸器専門医・指導医、 日本結核病学会結核・抗酸菌症認定医、 日本がん治療認定医機構がん治療認定医、 European Diploma in Adult Respiratory Medicine、 医学博士
医師の詳細はこちら
医師 部長
大槻 歩 (おおつき あゆむ)
OTSUKI Ayumu
日本内科学会認定内科医、 日本内科学会総合内科専門医、 日本呼吸器学会専門医・指導医、 日本呼吸器内視鏡学会気管支鏡専門医・指導医、 厚生労働省「医師の臨床研修に係る指導医講習会」修了
医師の詳細はこちら
医師 京橋クリニック副院長・呼吸器内科顧問 兼務
金子 教宏 (かねこ のりひろ)
KANEKO Norihiro
日本呼吸器学会専門医・指導医、 日本呼吸器内視鏡学会気管支鏡専門医・指導医、 日本アレルギー学会専門医・指導医(内科)、 日本内科学会認定内科医、 日本禁煙学会専門医・指導医、 産業医、 ICD(インフェクションコントロールドクター)
医師の詳細はこちら
医師 呼吸器外科 顧問/在宅診療科 兼務
杉村 裕志 (すぎむら ひろし)
SUGIMURA Hiroshi
呼吸器外科専門医合同委員会呼吸器外科専門医、 日本外科学会外科専門医、 日本胸部外科学会認定医、 日本がん治療認定医機構がん治療認定医、 Da Vinci console surgeon certificate
医師の詳細はこちら
医師 腫瘍内科 部長
大山 優 (おおやま ゆう)
OYAMA Yu
日本内科学会認定内科医・総合内科専門医、 米国腫瘍内科専門医、 米国血液科専門医、 日本臨床腫瘍学会指導医、 日本臨床腫瘍学会がん薬物療法専門医、 日本臨床腫瘍学会協議員、 日本臨床肉腫学会理事、 日本サルコーマ治療研究学会評議員
医師の詳細はこちら
医師 放射線科 部長・放射線治療センター長
庄司 一寅 (しょうじ かずふさ)
SHOJI Kazufusa
日本放射線腫瘍学会・日本医学放射線学会 放射線治療専門医、 厚生労働省指定オンライン診療研修修了
医師の詳細はこちら
医師 救命救急科 部長(画像診断担当)
伊藤 憲佐 (いとう けんすけ)
ITO Kensuke
日本核医学会PET核医学認定医、 日本専門医機構認定放射線科専門医、 日本医学放射線学会放射線診断専門医、 厚生労働省「緩和ケア研修会」修了
医師の詳細はこちら
※患者数は検査入院除く
※手術件数は1患者に対する複数回手術もカウントしている
| 男性 | 243人 |
|---|---|
| 女性 | 110人 |
| 計 | 353人 |
男女別患者割合
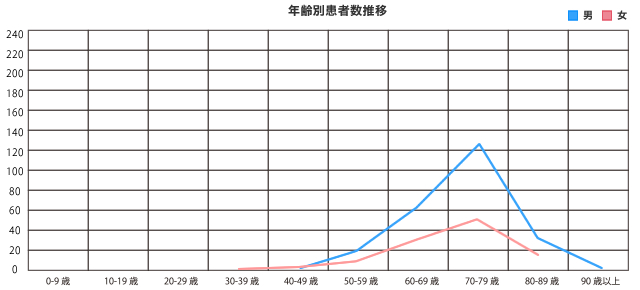
| 0〜9歳 | 0 |
|---|---|
| 10〜19歳 | 0 |
| 20〜29歳 | 0 |
| 30〜39歳 | 0 |
| 40〜49歳 | 2 |
| 50〜59歳 | 20 |
| 60〜69歳 | 61 |
| 70〜79歳 | 125 |
| 80〜89歳 | 34 |
| 90歳以上 | 1 |
| 合計 | 243 |
| 0〜9歳 | 0 |
|---|---|
| 10〜19歳 | 0 |
| 20〜29歳 | 0 |
| 30〜39歳 | 1 |
| 40〜49歳 | 2 |
| 50〜59歳 | 8 |
| 60〜69歳 | 31 |
| 70〜79歳 | 52 |
| 80〜89歳 | 16 |
| 90歳以上 | 0 |
| 合計 | 110 |
| 外来 | 1536件 |
|---|---|
| 入院 | 201件 |
| 外来 | 277件 |
|---|---|
| 入院 | 83件 |
| 肺がん患者数 | 353件 |
|---|---|
| その他の患者数 | 1175件 |
5大がん診療実績からみた肺がん患者数割合
肺がんの診断には、気管支鏡下あるいはCTガイド下生検が主に行われます。気管支鏡で安全に検査ができると判断した場合は外来で施行させて頂きます。一方で、当院においては、より正確な病理診断及び病期分類を目指している故に、以前にも増して検査手技の難易度が高くなってきています。気管支鏡での検査であっても合併症の可能性があったり、CTガイド下生検は入院して頂きます。合併症が認められなければ、通常は一泊二日となります。検査によっては例外がありますので担当医にご確認ください。
肺がんの脳転移を制御することは患者さまの全身状態を保ち治療を継続する上で非常に重要です。特に小細胞肺がんは化学療法や放射線療法に感受性の高い肺がんであり、脳転移に対しても放射線療法は非常に効果的です。昨今、小さな脳転移であれば、定位放射線治療やガンマナイフが行われますが、大きいものや個数の多い場合は全脳照射を行います。また限局型小細胞肺がん(胸に限局しているもの)に対し化学療法と胸部放射線療法が同時に実施され、非常に効いた場合には予防的全脳照射を行うことで生存が延びることがわかっています。ただし、予防的なものを含め全脳照射の実施に際しては、年齢や認知機能などを総合的に考慮した上で決めることになります。
喫煙者の肺がんの発生は非喫煙者に比べて約4倍から10倍といわれています。そのため、肺がんを防ぐには、禁煙が最も有効であるといわれています。また、喫煙者であっても、禁煙することにより肺がんの発生率を低下させることができます。しかし、近年では非喫煙者の肺がんが増加しており、原因は定かではありませんが、受動喫煙や生活習慣が関与しているかもしれません。
近年、非喫煙者の肺がんが増えてきており、そのほとんどが非小細胞肺がんの中の肺腺がんです。おそらくは受動喫煙環境(非喫煙者が喫煙者の煙を常日頃から吸引するような環境)が影響していると思われます。心配な方はドック検診や呼吸器内科・呼吸器外科の受診をお勧めします。
現在、高齢者肺がんの定義は75歳以上になっており、暦年齢だけで手術の可否を決定することはありません。暦年齢ではなく見た目年齢も重要視しています。術中・術後に危険因子となる併存症の有無も手術適応を決める上で重要になります。肺機能検査で1秒量(強制的に1秒間に吐く息の量)が1リットル以上であることが肺切除行うための目安にはなりますが、肺区域切除・肺部分切除などの肺縮小手術が可能なケースもあり、その場合にはその限りではありません。詳細は診察時にご相談ください。
早期の肺がんは原則手術を行います。医学的な理由により手術に耐えられない患者さまには、定位放射線療法や凍結療法を行います。 当院で行っているレーザー治療は主に光線力学療法(PDT; Photo dyanamic Therapy)という低出力レーザー治療で2014年に導入しています。早期の中枢型肺がんに対するPDTの治療成績は非常に良好です。また肺がんが進行し太い気管支に及ぶと呼吸をするための空気の通り道が狭くなって呼吸困難が出現し、患者さまの生活の質が著しく低下します。そのような場合にも症状緩和を目的としたPDTを行うことがあります。PDTを希望される方は診察の際に医師にご相談ください。また他の方法として、気道ステント・高周波・アルゴンプラズマ凝固焼灼術(APC)・バルーンなどを用いた気道拡張術にも呼吸器外科と協力して取り組んでいます。
術後早めに動いてもらうことによって、術後合併症の予防や日常生活への早期復帰につながります。 そのため、術後早期からの活動を促すために専任の理学療法士によりリハビリテーションが行われています。